
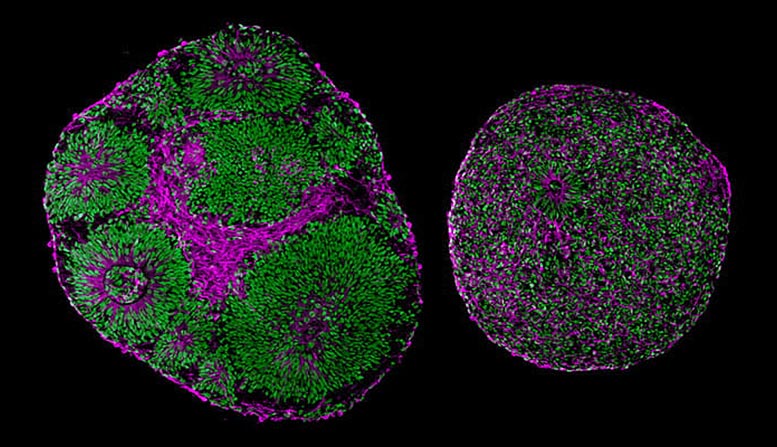
تكشف الصور المجهرية عن اختلافات كبيرة في الحجم والهيكل بين أشباه الدماغ المشتقة من متلازمة بيت هوبكنز (على اليمين) والسيطرة (على اليسار). الائتمان: العلوم الصحية بجامعة كاليفورنيا في سان دييغو
تستخدم دراسة جامعة كاليفورنيا ، سان دييغو (UCST) أنسجة دماغية بشرية مطورة معمليًا لتشخيص التشوهات العصبية في متلازمة بيت هوبكنز ومعدات العلاج الجيني التجريبية.
في دراسة نشرت في المجلة 02 مايو 2022 التواصل الطبيعياستخدم العلماء في كلية الطب في سان دييغو بجامعة كاليفورنيا ، بيركلي ، عضويات دماغ الإنسان لاكتشاف كيف أن التعديل الجيني المرتبط بالتوحد الشديد يعطل نمو الأعصاب. أدى استخدام أدوات العلاج الجيني لاستعادة وظيفة الجين إلى استعادة الجهاز العصبي والوظيفة بنجاح.
تم ربط العديد من الاضطرابات العصبية والنفسية العصبية ، بما في ذلك اضطرابات طيف التوحد (ASD) والفصام ، بطفرات في عامل النسخ 4 (TCF4) ، وهو جين أساسي في نمو الدماغ. تتحكم عوامل النسخ عند تنشيط أو تعطيل الجينات الأخرى ، لذا فإن وجودها أو عدم وجودها يمكن أن يكون له تأثير الدومينو على الجنين النامي. ومع ذلك ، لا يُعرف الكثير عما يحدث للدماغ البشري عند حدوث ذلك TCF4 تغير.
لاستكشاف هذا السؤال ، ركز الباحثون على متلازمة بيت هوبكنز ، وهي اضطراب يتميز بالتوحد. TCF4. يعاني الأطفال المصابون بحالة وراثية من إعاقات إدراكية وحركية عميقة ويكونون عاجزين عن الكلام بشكل عام.
متلازمة بيت هوبكنز (PTHS) هو اضطراب وراثي نادر يتميز بالتأخر في النمو ، والصرع ، وملامح الوجه المميزة ، وفرط التنفس المحتمل المتقطع بعد الاختناق. كما تم اكتشاف الكثير عن بيت هوبكنز ، فإن الطيف التطوري للاضطراب آخذ في التوسع ، بما في ذلك صعوبات التوحد والقلق واضطراب فرط الحركة ونقص الانتباه والاضطرابات العاطفية. يرتبط بخلل داخل الكروموسوم 18 ، خاصةً مع عدم كفاية التعبير عن جين TCF4.
فشلت نماذج الفئران الحالية لمتلازمة بيت هوبكنز في عكس الخصائص العصبية للمرضى بدقة ، لذلك طور فريق جامعة كاليفورنيا في سان فرانسيسكو نموذجًا بحثيًا بشريًا بدلاً من ذلك. باستخدام تقنية الخلايا الجذعية ، تم تحويل خلايا جلد المرضى إلى خلايا جذعية ، والتي تم تطويرها بعد ذلك إلى عضيات دماغية ثلاثية الأبعاد أو “أدمغة صغيرة”.
كشف الاختلافات الهيكلية والوظيفية بين الملاحظات المبكرة لعضويات الدماغ. TCF4النماذج المعدلة وضوابطها.
قالت أليسون آر ، الأستاذة في كلية الطب بجامعة كاليفورنيا في سان دييغو ومديرة وعضو مشروع الخلايا الجذعية بجامعة كاليفورنيا في سان دييجو: “حتى بدون المجهر ، يمكنك معرفة أي عضيات الدماغ يتحور”. قال ميوتري. اتحاد سانفورد للطب التجديدي.
ال TCF4كانت العضيات المحولة أصغر بكثير من العضيات العادية ، ولم تكن العديد من الخلايا في الواقع خلايا عصبية ، بل كانت نواقل عصبية. تتكاثر هذه الخلايا البسيطة ثم تنضج لتصبح خلايا دماغية متخصصة ، ولكن في العضيات المتحولة ، انحرف جزء من هذه العملية.
كشفت عن طريق سلسلة من الاختبارات TCF4 أدت الطفرة إلى تنظيم المصب SOX الجينات ومسار Wnt هما إشارات جزيئية مهمة توجه تكاثر الخلايا الجنينية ، والنضج إلى الخلايا العصبية ، والهجرة إلى المكان الصحيح في الدماغ.
بسبب هذا التنظيم ، لا تتكاثر السلائف العصبية بكفاءة ، وبالتالي تنتج عددًا أقل من الخلايا العصبية القشرية. الخلايا التي تنضج لتصبح خلايا عصبية أقل نشاطًا من الطبيعي وتميل إلى التجمع معًا بدلاً من تنظيم نفسها في دوائر عصبية مضبوطة بدقة.
قال المؤلفون إن هذه البنية الخلوية الغريبة قد عطلت تدفق الوظيفة العصبية في العضيات الدماغية المشوهة ، مما ساهم في ضعف الوظيفة الإدراكية والحركية.
قال فابيو بابس ، دكتوراه ، أستاذ مشارك في جامعة كامبيناس وباحث زائر في جامعة كاليفورنيا: “لقد اندهشنا لرؤية مثل هذه القضايا التنموية واسعة النطاق بهذا الحجم ، ونتساءل عما يمكننا فعله لمعالجتها”. أشرف على العمل بالتعاون مع مدرسة سان دييغو للطب ، مودي. لدى الأطفال ابن عم مصاب بمتلازمة بيت هوبكنز ، مما دفعه إلى القراءة TCF4.
اختبر الفريق طريقتين مختلفتين للعلاج الجيني لاستعادة الجين الوظيفي في أنسجة المخ. كلتا الطريقتين زادت بشكل فعال TCF4 المراحل ، وبذلك تم تصحيح الأنماط الظاهرية لمتلازمة بيت هوبكنز في القياسات الجزيئية والخلوية والكهربية.
وقال موتري “إنه لأمر مدهش أن نتمكن من إصلاح هذا الجين وأن الجهاز العصبي بأكمله يعيد تأسيس نفسه حتى على المستوى الوظيفي”.
يلاحظ ميوتري أن هذه التدخلات الجينية تحدث في مرحلة ما قبل الولادة من نمو الدماغ ، بينما في البيئة الطبية ، يتلقى الأطفال التشخيص والعلاج بعد بضع سنوات. لذلك ، يجب أن تؤكد التجارب السريرية أولاً ما إذا كان التدخل الأخير لا يزال آمنًا وفعالاً. يقوم الفريق حاليًا بتطوير معدات العلاج الجيني المرخصة مؤخرًا استعدادًا لمثل هذه التجربة ، حيث سيعيد الحقن الشوكي لناقل الجينات وظيفة TCF4 في الدماغ.
وقال موتري: “بالنسبة لهؤلاء الأطفال وأحبائهم ، فإن أي تحسن في الوظيفة الإدراكية الحركية ونوعية الحياة يستحق كل هذا الجهد”.
قالت أودري دافيدو ، رئيسة مؤسسة بيت هوبكنز للأبحاث: “ما يهم حقًا في هذه الدراسة هو أن هؤلاء الباحثين يتجاوزون المختبر ويعملون بجد لترجمة هذه النتائج إلى عيادات. هذا هو القياس.
ملاحظة: فابيو بابيز ، أنطونيو ب. كاميركو ، زينه س. دي سوزا ، فينيسيوس م. كارفالهو ، رايان أ. Seto ، Erin Lamontane ، “نشاط عامل النسخ 4 مرتبط بالإعاقات الوظيفية الخاسرة. Barbara MP Arajujo، Palo ENF Velho، Gabriel G. Hadat and Alison R. 2 May 2022، التواصل الطبيعي.
DOI: 10.1038 / s41467-022-29942-w
المؤلفون المشاركون: Zainana S. دي سوزا ، ريان أ. سيتو ، إيرين لامونتاني ، سيموني هـ. أفونسيني ، ساندرا م. سانشيز سانشيز ووي وو وهونغ ياو وغابرييل حدت موجودون في جامعة سان دييغو ؛ أنطونيو ب. كاميركو ، فينيسيوس م. كارفالو ، خوسيه ر. ديكسيرا ، دييغو س. Nagahara ، كارولينا ن. سانتو ، باربرا النائب. أراوجو وبالو إنف كامبيناس في جامعة فيلهو.
تم تمويل هذا العمل من قبل المعاهد الوطنية للصحة (المنحة R01 MH123828) ، ومؤسسة Pit Hopkins Research Foundation ، ومؤسسة ساو باولو للأبحاث (منح 2020 / 11451-7 ، 2018 / 03613-7 ، 2018 / 04240-0). ) وشركة جينوم الطاقة الأمريكية (DE-AC02-05CH11231).
الإفصاحات: أليسون آر موتري هو المؤسس المشارك والمؤسس المشارك لـ TISMOO ، وهي شركة مكرسة للتحليل الجيني وتكوين أعضاء الدماغ البشري.

“متعصب التلفزيون. مدمن الويب. مبشر السفر. رجل أعمال متمني. مستكشف هواة. كاتب.”






More Stories
خريطة جديدة للمريخ تكشف عن “هياكل” مخفية تحت سطح المريخ
زوج من نفاثات البلازما الضخمة تندلع من ثقب أسود هائل | الثقوب السوداء
الأسمنت المستوحى من عظام الإنسان أصعب بخمس مرات من الخرسانة العادية